Reaksyon sa mga compound sa mercury
Ang metal nga mercury ug ang mga compound niini makahilo kaayo sa buhing mga organismo. Tinuod kini ilabi na sa mga compound nga matunaw sa tubig. Kinahanglan nga mag-amping pag-ayo kung mag-eksperimento sa mga kombinasyon niining talagsaon nga elemento (ang mercury mao lamang ang metal nga likido sa temperatura sa lawak). Pagsunod sa sukaranang mga lagda sa usa ka chemist? motugot kaninyo sa luwas nga pagpahigayon sa pipila ka mga eksperimento uban sa mercury compounds.
Sa una nga eksperimento, nakuha namon ang aluminyo amalgam (usa ka solusyon niini nga metal sa likido nga mercury). Mercury (II) nga solusyon Hg nitrate (V) Hg (NO3)2 ug usa ka piraso sa aluminum wire (litrato 1). Ang aluminum rod (maampingong gilimpyohan sa mga deposito) gibutang sa usa ka test tube nga adunay solusyon sa matunaw nga mercury salt (litrato 2). Human sa pipila ka panahon, atong maobserbahan ang pagpagawas sa mga bula sa gas gikan sa nawong sa wire (mga litrato 3 ug 4). Human makuha ang sungkod gikan sa solusyon, nahimo nga ang yutang kulonon gitabonan sa usa ka fluffy coating, ug dugang pa, nakita usab nato ang mga bola sa metal nga mercury (mga litrato 5 ug 6).
Chemistry - kasinatian sa paghiusa sa mercury
Ubos sa normal nga mga kondisyon, ang nawong sa aluminum gitabonan sa usa ka hugot nga haom nga layer sa aluminum oxide.2O3epektibo nga naglain sa metal gikan sa agresibo nga mga impluwensya sa kalikopan. Human sa paglimpyo ug pagpaunlod sa sungkod sa usa ka solusyon sa mercury nga asin, ang mga Hg ion gipapahawa2+ mas aktibo nga aluminum
Ang mercury nga gideposito sa ibabaw sa sungkod nagporma og usa ka amalgam nga adunay aluminum, nga nagpalisud sa oxide sa pagsunod niini. Ang aluminyo usa ka aktibo kaayo nga metal (kini nag-reaksyon sa tubig aron buhian ang hydrogen - ang mga bula sa gas naobserbahan), ug ang paggamit niini ingon usa ka materyal nga istruktura posible tungod sa dasok nga oxide coating.
Sa ikaduhang eksperimento, atong makita ang ammonium NH ions.4+ gamit ang reagent ni Nessler (ang German nga chemist nga si Julius Nessler ang unang migamit niini sa pagtuki niadtong 1856).
Eksperimento sa reaksyon sa mga hops ug mercury compound
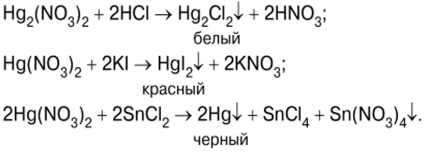
Ang pagsulay nagsugod sa pag-ulan sa mercury(II) iodide HgI.2, human sa pagsagol sa mga solusyon sa potassium iodide KI ug mercury (II) nitrate (V) Hg (NO3)2 (litrato 7):
Orange-pula nga precipitate sa HgI2 (litrato 8) dayon pagtratar sa sobra nga potassium iodide nga solusyon aron makakuha usa ka matunaw nga komplikado nga compound sa pormula K2HgI4 ? Potassium tetraiodercurate (II) (Larawan 9), nga mao ang reagent ni Nessler:
Uban sa resulta nga compound, atong makita ang ammonium ions. Ang mga solusyon sa sodium hydroxide NaOH ug ammonium chloride NH gikinahanglan gihapon.4Cl (litrato 10). Human sa pagdugang sa usa ka gamay nga kantidad sa ammonium salt solution sa Nessler reagent ug alkalizing sa medium nga adunay lig-on nga base, among nakita ang pagporma sa usa ka yellow-orange nga kolor sa sulod sa test tube. Ang kasamtangan nga reaksyon mahimong isulat ingon:
Ang resulta nga mercury compound adunay usa ka komplikado nga istruktura:
Ang labi ka sensitibo nga pagsulay sa Nessler gigamit aron mahibal-an bisan ang mga timailhan sa mga asin sa ammonium o ammonia sa tubig (eg tubig sa gripo).

